水生所在鱼类抗病毒天然免疫稳态调控研究中取得进展
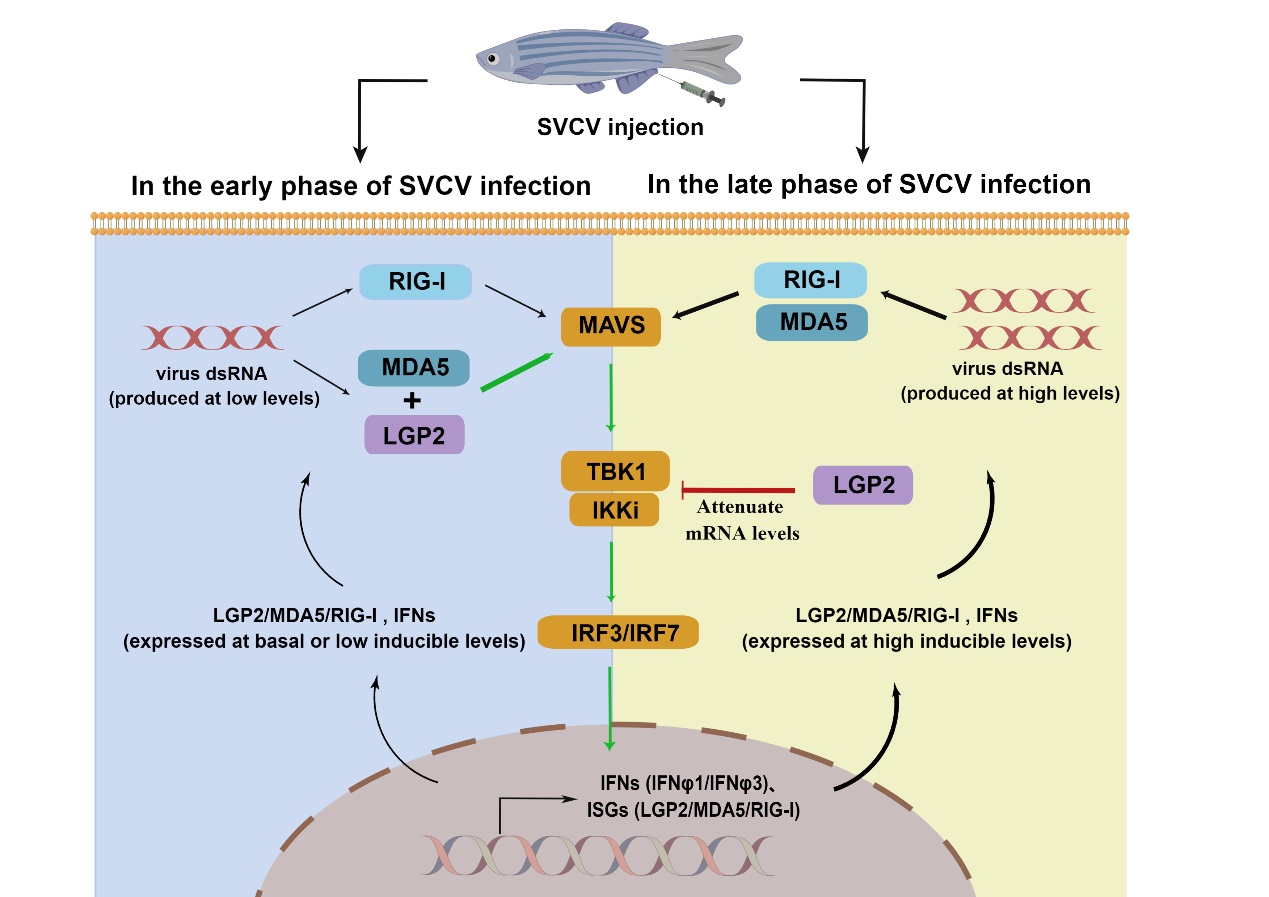
图1 斑马鱼LGP2在病毒感染的不同时期维持机体的免疫稳态以促进鱼体存活
快速识别病毒感染,启动机体的抗病毒免疫功能以清除病毒,在完成病毒清除后,及时终止免疫反应避免对组织细胞的过度损伤,是机体在应对病毒感染时成功存活的关键。在与病毒感染的长期博弈中,脊椎动物为了更胜一筹,演化出了复杂精细的免疫稳态调控机制。
2003年,具有识别病毒感染信号功能的胞浆RLR受体被成功鉴定,为深刻理解脊椎动物如何快速启动抗病毒免疫反应打开了一扇大门。RLR受体家族有3个成员,包括RIG-I、MDA5和LGP2。哺乳类的研究表明,RIG-I和MDA5分别识别不同病毒的感染信号,以激活机体的干扰素抗病毒免疫反应清除病毒。但是,LGP2发挥何种功能,至今仍充满谜团和争议。目前流行的观点认为:LGP2能协助MDA5识别病毒感染,从而促进机体的抗病毒免疫反应,但又抑制RIG-I介导的抗病毒免疫反应。这个观点有体外数据支持。但是,应对病毒感染时,LGP2为何既要促进又要抑制机体的免疫反应令人费解。此外,接连3个实验室对小鼠LGP2基因的敲除研究也出现了截然相反的结果。
鱼类也有3个保守的RLR受体。鱼类研究同样出现了LGP2或发挥正调控、或发挥负调控的矛盾结果。针对这种认知混淆的现状,中国科学院水生生物研究所张义兵研究团队在2018年提供体外证据:斑马鱼LGP2在病毒感染的早期能激活细胞的干扰素抗病毒免疫反应,发挥正调控功能;在病毒感染的晚期,则抑制细胞的抗病毒免疫反应,发挥负调控功能(J Immunol 2018; 200:688-703)。最近,团队又提供了体内证据:通过比较野生型和敲除LGP2基因的斑马鱼在感染病毒后的免疫反应,证明斑马鱼在缺失LGP2后死亡率显著增加。机制是:缺失LGP2严重破坏了鱼体在应对病毒感染时的免疫稳态。这种严重破坏,导致在病毒感染的早期,鱼体的干扰素抗病毒免疫反应不能尽快启动到有效清除病毒感染的适度水平,而在病毒感染的晚期,又不能使鱼体的抗病毒免疫反应及时回归到正常的本底水平;团队同时揭示了LGP2发生功能转换的分子机制(图1)。研究论文近期在IScience发表(IScience,2022, 25:104821)。
团队进一步证实了LGP2的功能在斑马鱼和人中的保守性,提供了在病毒感染的不同时期,斑马鱼和人的LGP2行使相同的双重调控功能、精确调控抗病毒免疫反应的分子证据。poly(I:C)是人工合成的双链RNA。通过用poly(I:C)模拟病毒感染细胞时产生的病毒核酸信号,采用滴定poly(I:C)转染细胞时的剂量来模拟病毒感染细胞的不同时期。研究发现:在模拟病毒感染的早期,LGP2通过促进MDA5快速启动细胞的干扰素抗病毒免疫反应以清除病毒;在模拟病毒感染的晚期,LGP2则反过来抑制RIG-I以及MDA5触发的信号通路,负调控细胞的抗病毒免疫反应,以使机体免疫反应恢复到正常的本底水平,最终维持机体的免疫稳态。研究结果近期于Frontiers in Immunology在线发表。团队的研究结果统一了对脊椎动物LGP2的功能认知,揭示了脊椎动物LGP2调控机体免疫稳态的分子机制、以及免疫稳态在机体抗病毒感染中的重要意义。
两篇在线论文的第一作者为博士研究生龚秀英,通讯作者为张义兵研究员,桂建芳院士在研究中给予具体指导。该研究得到国家重点研发计划、中国科学院战略先导科技专项和国家自然科学基金等课题的支持。
论文链接:https://doi.org/10.1016/j.isci.2022.104821
https://www.frontiersin.org/articles/10.3389/fimmu.2022.985792/full
