水生所等揭示我国克氏原螯虾主养殖区虾肠道抗生素抗性基因的分布及其影响规律
疾病给农业生产造成了巨大的经济损失。为治疗细菌性疾病,农业(特别是养殖业)生产中常常使用抗生素,但抗生素的使用会导致耐药菌株的产生,对生态环境安全乃至人类健康造成潜在的威胁。抗生素抗性基因(antibiotic resistance genes,ARGs)作为一种新兴环境污染物,是细菌耐药性的遗传基础,可导致条件致病菌产生耐药性,因而受到了广泛关注。水产养殖环境很复杂,种植业、畜牧业、人类医疗活动以及水产养殖业中的细菌病防治,都可能影响水产养殖中的抗生素抗性基因。但目前我国主要水产养殖区养殖动物肠道微生物,ARGs,特别是高风险ARGs的分布及其影响因素的研究还很缺乏。
克氏原螯虾(Procambarus clarkii)是重要的水产养殖品种。2020年我国克氏原螯虾养殖总面积达到2184万亩,养殖总产量达到239万吨。中国科学院水生生物研究所寄生虫学与协同进化学科组吴山功博士联合化学生态学学科组吴辰熙研究员以及兰州大学李欢青年研究员团队以克氏原螯虾为研究对象,对相关问题开展了系统研究。
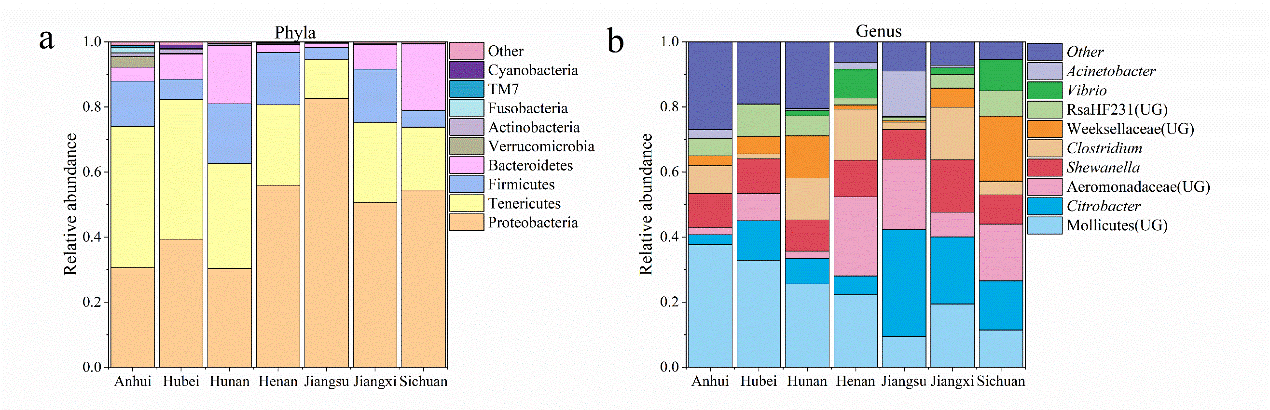
图1 克氏原螯虾肠道微生物组成 a,门水平;b,属水平
研究发现,在门水平上,克氏原螯虾肠道微生物以变形菌门(Proteobacteria)为主(图1a);属水平上,以柔膜菌(Mollicutes(UG))为主(图1b)。进一步分析发现江苏省和其他省份克氏原螯虾肠道微生物群落结构差异显著。
克氏原螯虾肠道中存在丰富的抗生素抗性基因,其中以β-内酰胺类抗性基因的丰度最高,其次是四环素抗性基因。栖息地、环境因素(NO3-N、pH和水温)和微生物α多样性都对ARGs具有显著的影响。条件致病菌链球菌(Streptococcus)、气单胞菌(Aeromonas)和不动杆菌(Acinetobacter)与高风险ARGs呈显著正相关,说明这些条件致病菌可能是高风险ARGs的潜在宿主,可能导致水产养殖中抗生素治疗无效,因而需要对病原微生物进行药敏实验以指导合理用药。
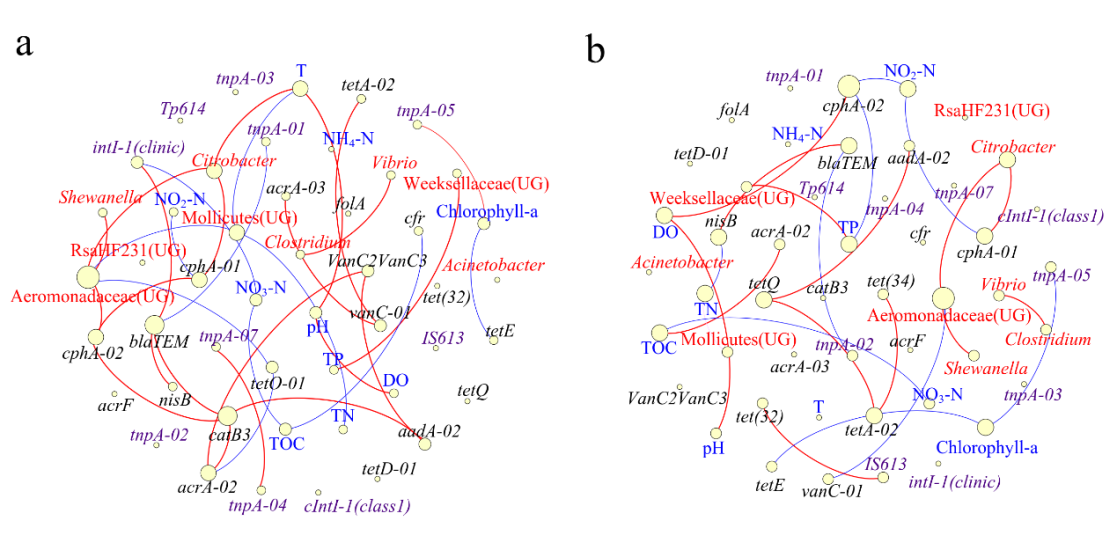
图2 环境因子、微生物、MGEs和ARGs的共现网络(a,绝对丰度;b,相对丰度)
环境因子、优势肠道细菌、MGEs和高丰度ARGs之间的共现模式研究发现,大部分ARGs与环境因子、MGEs和微生物呈现显著的正相关(图2a和2b)。此外,研究还发现,有些抗性基因是高度临床医疗相关的基因,说明克氏原螯虾肠道抗生素抗性基因可能不全是水产养殖用药引起的。研究结果为水产养殖中细菌性疾病的用药、ARGs的风险管理和评估,以及相关措施的制定提供一定的依据。
该项工作以“Distribution and influencing factors of antibiotic resistance genes of crayfish (Procambarus clarkii) intestine in main crayfish breeding provinces in China”为题在线发表于Science of The Total Environment。水生所吴山功副研究员为论文通讯作者,兰州大学硕士研究生完颜瑞军、水生所与大连海洋大学联合培养硕士研究生潘美井为论文共同第一作者。该研究得到国家重点研发计划(2020YFD0900303)等项目的资助。
论文链接:https://www.sciencedirect.com/science/article/pii/S0048969722067110?via%3Dihub
