水生所建立鱼类诱导性Treg技术提升鱼类借腹生殖效率
通过性腺原基或生殖干细胞移植借腹生殖,以实现供体配子的加速成熟,是鱼类育种领域的一项重要技术。然而,移植体往往受到受体鱼的免疫排斥,导致借腹生殖效率低下。2025年,诺贝尔生理学或医学奖授予了一项有关“Foxp3介导的调节性T细胞(Tregs)维持免疫耐受”的成果。能否建立鱼类诱导性Treg(iTreg)技术,培育免疫耐受受体鱼,以克服其对移植体的免疫排斥呢?
中国科学院水生生物研究所孙永华团队瞄准这一目标开展研究。前期,他们发现Foxp3a而非Foxp3b是介导斑马鱼中Tregs功能的核心转录因子,其突变导致性腺分化中的免疫稳态失衡和精子发生障碍(Li et al., Journal of Genetics and Genomics, 2020,封面论文);进一步建立了基于诱导性原始生殖细胞(iPGC)和生殖干细胞移植的鱼类跨物种借腹生殖技术(Wang et al.,Nature Communications, 2023; Zhang et al.,Science China Life Science, 2022)。
近日,孙永华团队通过构建foxp3a转基因斑马鱼,成功建立了鱼类iTreg介导的免疫耐受技术,突破了异体性腺原基皮下移植(SGPT)和生殖干细胞腹腔移植(IGCT)的免疫排斥障碍,显著加速了供体配子的产生和品系构建。
团队构建了转基因斑马鱼品系Tg(CMV:foxp3a),其表现出iTreg介导的免疫耐受特性。当他们将异体来源的性腺原基移植至野生型斑马鱼的皮下组织,所有的移植体均被彻底清除;反之,当以免疫耐受斑马鱼作为移植受体时,供体性腺原基在受体皮下高效定植和增殖,形成膨大的性腺组织(图1A–C)。更重要的是,供体生殖细胞在2月龄的受体中进行着超快速的精子发生,仅需约1个月左右即可成熟和产生子代(图1D–F)。
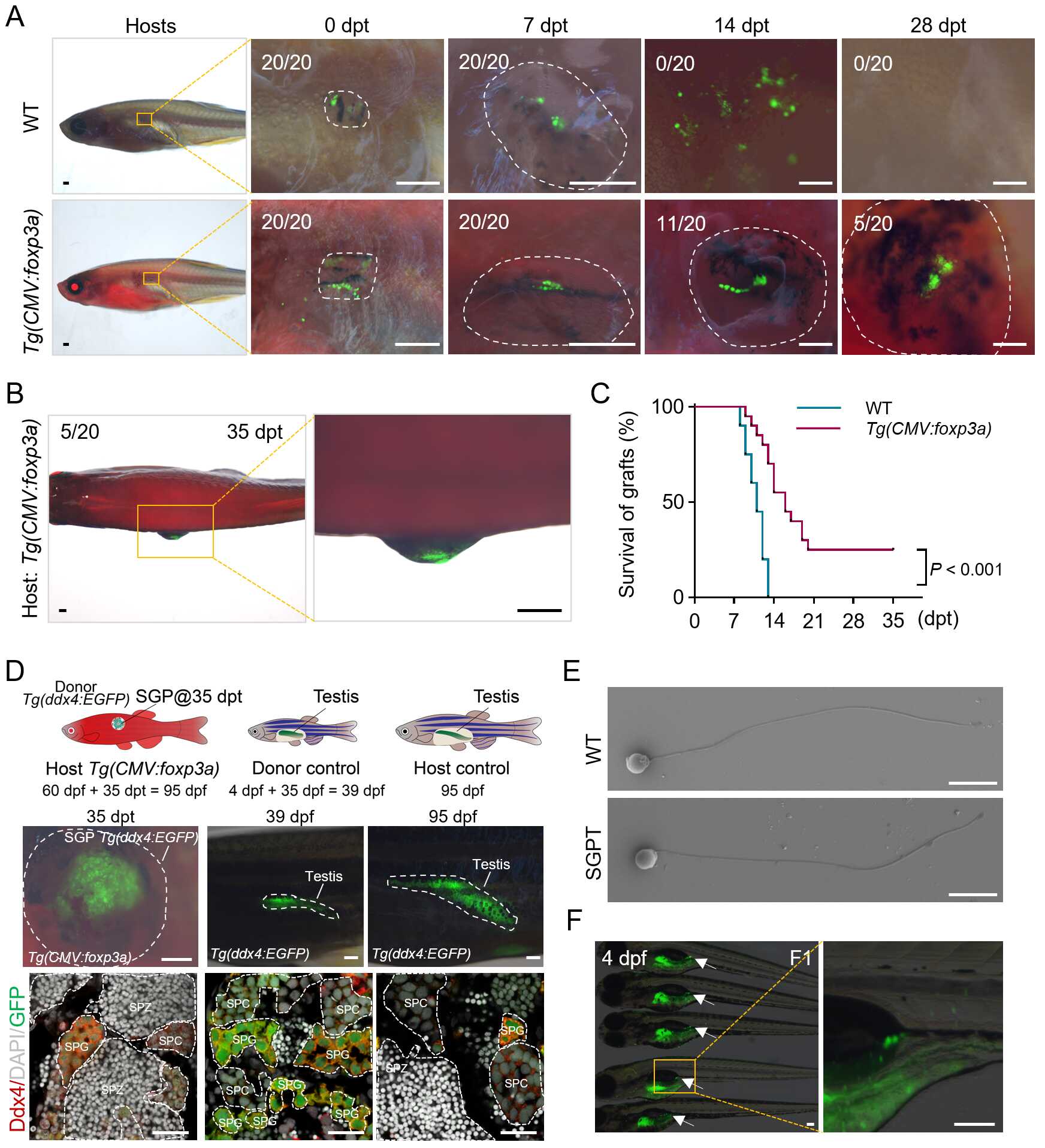
图1 利用iTreg免疫耐受斑马鱼突破异体性腺原基移植障碍和配子超速发生
同时,这一策略也可以显著提升IGCT的效率。相比传统至少3个月的F1代构建周期,利用iTreg技术仅需1个月即可完成,效率得到显著提升(图2)。
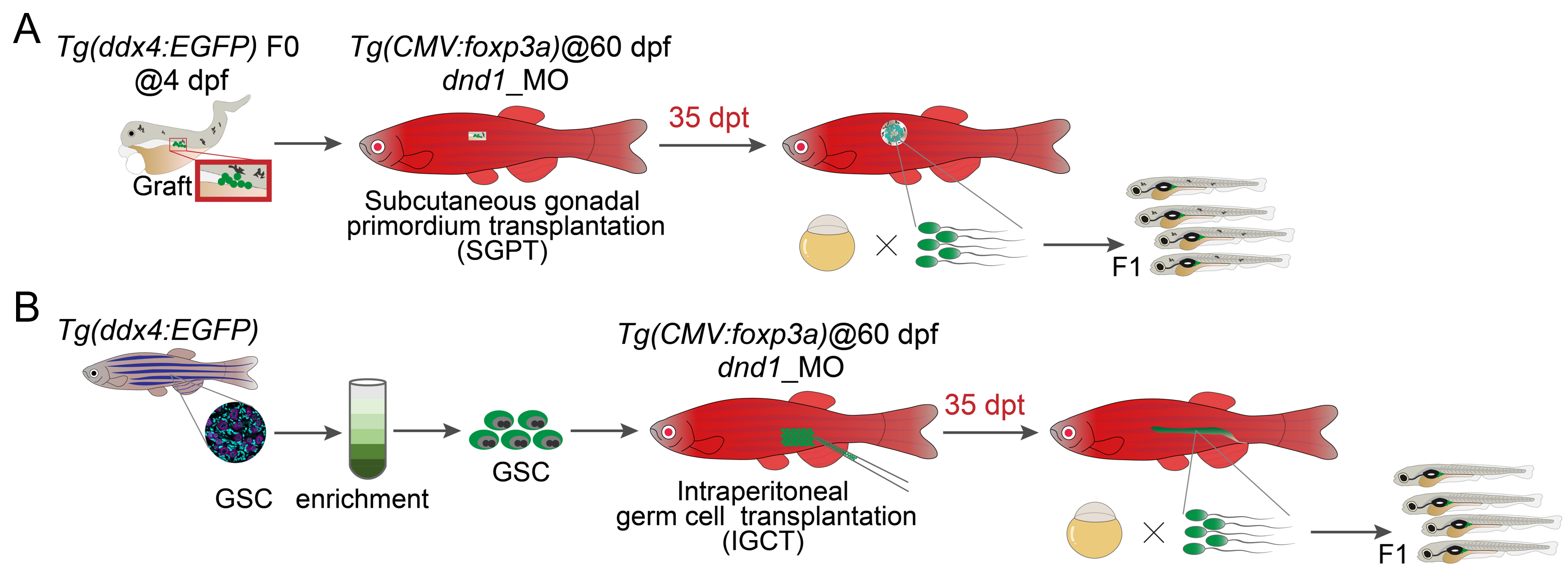
图2 利用iTreg免疫耐受鱼实现SPGT和IGCT介导的品系超速构建示意图
总之,该研究首次建立了鱼类中iTreg技术,攻克了同种异体性腺原基移植中的免疫排斥难题,实现了供体配子的超速成熟。这一突破也为鱼类借腹生殖的效率提升和未来应用奠定了免疫调控基础。
上述成果以“在斑马鱼中利用foxp3a过表达建立Tregs介导的免疫耐受突破异体移植障碍”为题,在线发表在国际学术期刊Journal of Genetics and Genomics。水生所博士生祝俊雯和郝永康为该论文共同第一作者,孙永华研究员和王小四副研究员为通讯作者。相关工作得到国家杰出青年科学基金、国家重点研发计划项目等资助。文中所构建的转基因品系(CZ2204)已保藏于国家水生生物种质资源库国家斑马鱼资源中心。
原文链接:https://doi.org/10.1016/j.jgg.2026.02.024
参考文献
Hori, S., Nomura, T., Sakaguchi, S. (2003). Control of regulatory T cell development by the transcription factor Foxp3. Science 299: 1057-1061
Wang, X., et al. (2023). Induced formation of primordial germ cells from zebrafish blastomeres by germplasm factors. Nat. Commun. 14: 7918
Zhang, F., et al. (2022). Surrogate production of genome-edited sperm from a different subfamily by spermatogonial stem cell transplantation. Sci. China Life Sci. 65: 969-987
Li, X., et al. (2020). A critical role of foxp3a-positive regulatory T cells in maintaining immune homeostasis in zebrafish testis development. J. Genet. Genomics 47: 547-561
